编者按:新型冠状病毒能否自己在家采样,通过类似试纸的简易工具自我检测?随着全球疫情的发展,居家隔离变成常态,自我检测的需求也随之产生。5月14日,北京大学教授、北京大学生物医学前沿创新中心副主任黄岩谊在科学公益组织未来论坛发起的第十期“《理解未来》科学讲座:病毒与人类健康-专题科普”上总结了目前各类新冠检测方法的实际困难和改进方向。
首先,我们要了解新冠病毒的检测主要分为核酸检测和抗体检测,这两个检测方法完全不一样,目的不同,采样不同,方法不同,结果解读不一样,适用范围也不同。
核酸检测的最常见样本是鼻咽拭子,采样需要专业手法。 黄岩谊介绍道,一个多月前,华西医院提出了用唾液进行新冠诊断的可能性。这是一个比较容易实现自我采样的操作。美国FDA也已批准用在家采集的唾液样本用于新冠检测。
此外,美国耶鲁大学比较了唾液和鼻咽拭子PCR核酸检测的效果。实验结果表明,和鼻咽拭子比,唾液采样的稳定性相当不错,甚至更好一些。这是一个很好的起点。
“唾液采样是非常令人鼓舞的新方法,如果得到推广有望很好地解决我们过去采样中的面临的问题。”不过,这些样本依然需寄去检测中心。
抗体检测的岩本是血或血清,可以利用胶体金显色进行试纸检测方法,类似于验孕试纸。这个方法的好处是非常简单、易用、便宜,而且不需要复杂的设备,速度非常快。
横向来看,各国目前的抗体检测手段并没有谁“一枝独秀”,无法具备和核酸检测一样稳定和优秀的特异性,尤其是胶体金测试的假阳性率是一个大问题。
最后,黄岩谊介绍了与合作团队开发的超越核酸检测的RNA测序法,大大降低了实验操作难度,可以使实验结果更加稳定、可靠和快捷获取。在此基础上,研究人员观察到了有趣的突变信息。
演讲全文由中科院生物物理所博士生李敏、郭丽洁整理。澎湃新闻经授权后二次整理、发布。
黄岩谊:新型冠状病毒的实验室检测
我本人并不在第一线从事新冠感染的诊断,而主要是发展新的方法学来改善现在病毒测序碰到的一些实际困难。

前不久美国疾控中心发布新的冠状病毒的集体照,蓝色标出来的是病毒颗粒,病毒颗粒里的小黑点就是切开了的断面上的核酸,就是这些冠状病毒里包含了基因组的部分。这个基因组对于我们做检测有极其重要的意义,是我们检测的物质基础。
分子诊断对于疾病诊断来说是重要的组成部分,疾病诊断是复杂问题,尤其是新疾病出现的时候,对于一个传染病来说,已知病原体的情况下分子诊断成为极为重要的指标。它的主要目的有以下几个:第一,它确定临床症状,比如发烧是否是由新冠病毒引起的,避免它和其他疾病混淆起来。第二,对疾病的进程进行定性(比如阳性阴性)或者定量描述,比如病毒载量的多少。第三,从更加精细的角度出发,某些分子诊断还可以提供疾病的治疗方案,帮助确定它的方案,提供证据的支撑。第四,从病毒疾病的角度出发,可以追踪变异情况,这也非常重要,研究并且预测病毒在传播过程中的传染和致病能力的演化。
什么是分子诊断?狭义的分子诊断一般来说就是核酸检测。核酸检测是指检验样品中间是否含有特定序列的DNA或者RNA的片段,作为病原微生物存在的证据。

除此之外我们针对抗体做检测就是抗体检测,抗体检测看的不是病毒本身,而是看血液中间或者体液中间有没有抗体分子的出现。
还有一种检测是抗原检测,目标是病毒身上的物质,比如我们上图中看到的蓝色标记的这两个地方,这两个都是病毒独有的蛋白,刺突S蛋白和核衣壳N蛋白,看他们是否存在于样品中,就是抗原检测。

检测,归根到底是针对分子的测量,测量分子数量的多少;这是由病毒本身的结构和组成来决定的,都有其物质基础。从检测上讲,除了核酸分子(上图中绿色箭头标出来的),它是每个病毒里有一条分子外,还有很多蛋白质分子(几个红色箭头标出来的),在病毒里数量很多。但是这些分子的数目分布还是有区别的,S蛋白,大概每个病毒有上百个;N蛋白和M蛋白每个病毒有上千个。对这些数量的了解非常有助于我们今后发展特异性的检测技术来确定病毒的存在。
关于检测,国家卫健委的通报和药监局的审批一直都是围绕核酸和抗体进行。这两个检测方法完全不一样,目的不同,采的样品来源不同,检测方法不同,结果解读不一样,适用范围也不同。下面稍微介绍一下这两个方法。
核酸检测
核酸检测,首先是采样。
要确保采样成功有两个关键,一个是使用的材料即拭子是有讲究的,不是随便一个棉签就可以;同时,拭子采样后的保存环境也是有讲究的。
另外采样本身的操作是有讲究的,手法也重要,也不能过去一捅就能够采到。举个例子,最常见的样品就是鼻咽拭子,注意采样的拭子要一直伸到鼻咽部的最后面,在口咽部的上方。这不是一个很容易的操作,很讲究经验和手法,自己做也是有困难的,一般也不推荐自己这么采样。还有喉咽拭子,张开嘴,也是要将很长的拭子深入到口腔后部,在咽喉部位,扁桃体边上。这个取样也不是自己可以简单做的,通常还要把舌头压下去。
采样部位的不同反映在检测结果上也不一样,中国科学家们很早就总结了一些规律。
比如,随着(出现症状之后)时间增加,采样得到的核酸数量越来越少。另一个结果,鼻咽拭子采到的核酸量会比喉咽拭子高一些,稳定性也稍微好一些。早期得到的经验对后面指导采样的流程有重要的意义,就是应该怎么采、采什么地方的样品。
疾病的特点导致了病毒侵染部位有特点,既有偏好,也受发病时间的影响。实际上,作为检测,可以用各种样品,不仅仅只是两种拭子。第七版的诊疗方案中明确提出了鼻咽拭子、痰、其他下呼吸道分泌物、血液、粪便的标本中都可以测出病毒核酸。还有调查研究表明,这么多的论文总结起来,看上去在很多样品中比如眼泪、粪便中都可能检测到核酸病毒,但这里面痰液或下呼吸道分泌物是最不容易漏检的,也就是检出率是最高的,接下来就是鼻咽拭子。
样品采集后做检测,第一步通常是核酸提取,就是把样品中的核酸部分留下,其他部分杂质、人脱落的细胞、其他分子如蛋白质分子等等都除掉。
通常的核酸提取,采用的都是把核酸分子用和它亲和力强的材料先吸附;等到把其它物质都分离掉后,在把吸附的核酸分子洗脱下来,实现了提取,同时也是纯化和富集的步骤。在实验室里面,要么使用硅胶膜来吸附,要么利用表面修饰的磁性小颗粒来实现吸附。这两个方法现在在新冠病毒的核酸检测中,都广泛使用。
核酸提取之后是扩增的步骤,这是通过厂家提供的几管试剂实现的。上图中左边是华大基因的试剂,里面是几个小试管,右边是美国疾控中心分发的试剂。检测的过程叫做RT-PCR,就是逆转录-聚合酶链式反应。这是一个利用自然中存在的核酸复制机制来实现DNA分子的体外复制的操作,已经发明了近四十年,是分子诊断的基础技术,也是现代生物学和医学进步的重要奠基性技术。
在每一个试管中,除了加待测样品就是核酸提取液外,还要加DNA聚合酶,逆转录酶,以及引物和探针。新冠病毒是RNA病毒,病毒里面包裹这一条基因组RNA,通过逆转录酶把这条RNA变成和它互补的DNA,然后再复制一遍,变成双链DNA,再往后就可以通过热循环一遍一遍的解开配对的双链,分别复制。1变2、2变4、4变8,经过N轮循环,理论上可以得到几何级数增长的特定片断的DNA。在复制的过程中,一个巧妙设计使每一次的复制能产生特定的荧光分子,复制的分子越多产生的荧光越多,我们就可以检测到这信号,这样一轮一轮的复制下去,我们看荧光增长。如果有荧光增长就是有待测物质,即所谓阳性;没有增长就是没有待测物质即所谓的阴性。荧光增长越快,就说明分子越多,增长越慢,说明分子越少,大概就这样一个过程。
另外,选择探针序列也就是引物序列非常讲究,在大概3万个碱基左右长度的序列,检测哪一段还是需要下一番功夫的。
一组韩国科学家,前不久发表了一个对比结果,把一月份就分别采用的核酸检测的检测位点,的有效性做了一个相对客观的比较。各国科学家确定的用来做诊断的位点,是有区别的。上面这里,我标出了这些检测的核酸片段在基因组中的位置,比如中国的两个位点,一个是ORF1ab,另一个是N;而美国的三个,都在N蛋白基因上;德国的,一个在RdRp基因上,一个在E基因上。

上图是N基因的一段序列,里面用颜色表示的是,各个国家检测的位点,所使用引物的位置。可以看出,少量位置,各个国家的科学家们确定的有一些小的重叠,但是总的来说,并不是精确在一起。结果很有意思,韩国科学家的对比实验提出来,中国和美国选择的位点是这些检测中灵敏度最高的,这也从侧面反映了我们科学家早期选择位点的时候选的很准,这是需要经验的,需要能力,也需要做出科学判断的。
核酸检测是否还可以改进?首先看速度,一个标准的核酸检测过程,取样是很快的,然后把它存到运送培养基里,把样品攒到一定数量的时候,集中灭活,56度、30分钟,然后进行核酸提取;核酸提取差不多30-90分钟,PCR反应40-60分钟,这个是可以一批样品,常常96个一起做的,出来之后可以快速结果判定,整个实验做下来大概小半天的样子。这个过程能不能加速?如果是单个样品,样品采集之后直接就做,可以跳过很多步骤,比如直接放到裂解液里面,然后做快速的核酸提取,甚至不做提取就做快速的PCR,这样可能在30分钟左右就拿到结果。可以看到,PCR检测本身是可以做到快速的,尤其是样品量少的时候可以这么做,但样品多的时候最好是一批一批地操作更有效率。
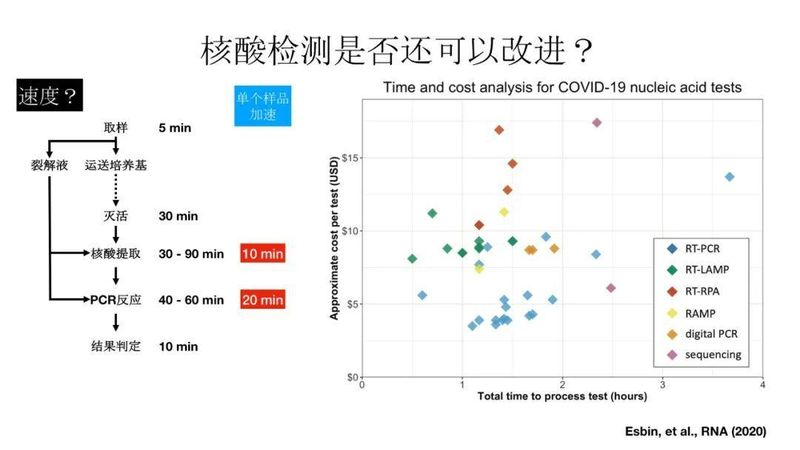
上图可以看到,各种方法检测所需的时间,大部分在一两个小时内都能做完,价格从几美元到十几美元。这里方法很多,有的已经不再是所谓RT-PCR方法,但还是充分借用了大自然的力量,利用自然界遗传物质的复制机制,进行特定的DNA片段的扩增,最终达到足够强的信号获取。
基于对检测速度的追求,即使是通过RT-PCR方法,为了减少操作上的技术壁垒和失误,可以采用所谓POCT的设备,也就是可以在现场使用的小型仪器装置。

上图中的两个是3月下旬的时候美国药监局最早批准紧急使用的两个仪器,分别可以在30分钟或45分钟内完成从样品到结果的检测全流程。在传染病流行期间利用这样的设备至少有两个重要好处,一个是分散处理病人检测需求,避免样品积压和运送困难。二是可以采用几乎全封闭的实验室设计,减少了操作者的生物安全风险。

上图的仪器可能是这一类检测仪器中最出风头的,这是美国超级销售特朗普亲自带货的小仪器,很可惜他没有摆对,图中不是正确的摆放方法。这个机器可以在5分钟之内给出阳性结果,十几分钟给出阴性结果,真正使用的时候整体所花的时间实际上会再长一些。要说明的是,这不是一个新的发明,不是有了新冠病毒突然就冒出了这么一个新发明。这个仪器已经在市面上很长时间了,在被新东家雅培买走之前,它已经是市场上用来检测流感病毒微生物的便携设备。
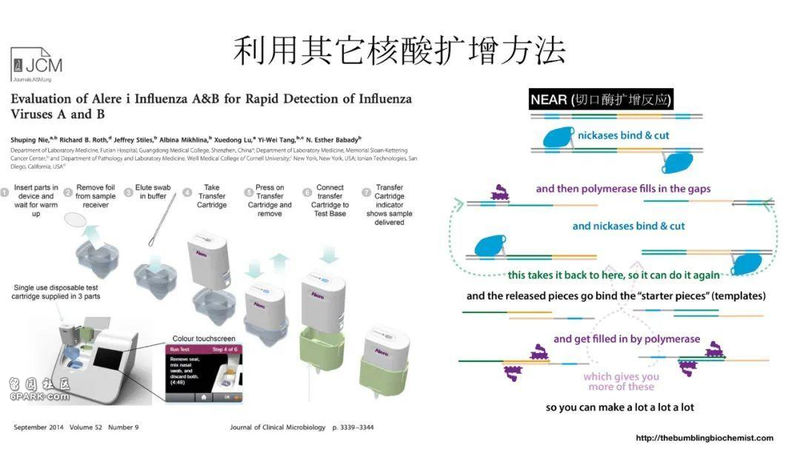
比如上图,这篇2014年深圳福田医院的科研人员参与的一篇论文,就是在评价这个仪器检测流感的表现。这个仪器用的基本技术是一个相对冷门的扩增方法,叫做NEAR(切口酶扩增反应),自然界存在很多奇奇怪怪的酶,可以做很多事情。切口酶就是在DNA切面上形成一个小切口,然后让聚合酶找到那个地方,可以开始做复制,不断的形成切口,不断的复制。这是非常巧妙的一个方法,不需要做PCR反应和热循环,属于等温扩增的一种。等温扩增的意思,是不需要做热循环,扩增过程在一个恒定的温度下进行,好处是这个过程变得非常简单;另一个好处是快,因为等温扩增的检测常常都是几分钟、十几分钟的时间尺度下完成的。
除了NEAR之外,还有很多等温扩增反应可以利用在核酸的检测上。例如一个相对比较有名的LAMP环介导等温扩增,这是日本科学家Notomi等人在2000年左右发明的,这个方法也是用四个或者六个引物序列加到待测物质里面,把它的温度稍微升一点,通常会在60度左右的温度下做等温扩增反应,不需要很复杂的仪器很快就能做完。这个方法的一个好处是,设备可以做的很简单,可以很容易操作,肉眼就可以做判别。
中国药监局也批准了基于这类反应的体外诊断试剂,例如这是成都博奥晶芯做的基于LAMP扩增方式的新冠病毒诊断设备。3月2号习总书记到清华考察的时候,程京院士给他展示的就是这个方法。
还有其他方法,其中一个方法是RPA,也是相对比较容易。它用两种酶的组合,重组酶和聚合酶放在一起,通过一个很复杂的循环,实现核酸分子的扩增,虽然复杂但是非常高效,非常快。基于RPA,在美国波士顿有名的华裔青年科学家张锋,把它和基因编辑结合在一起,嫁接起来实现了对RNA的检测,他们起了一个名字叫SHERLOCK(福尔摩斯的大名)还用这个名字注册了企业,来做这个试剂的开发。无独有偶,在美国加州旧金山,基于LAMP方法,嫁接基因编辑,Jennifer Donna跟她的合作者一起也做了一个新方法,叫做DETECTR,成立的公司叫做Mammoth Biosciences。这两个方法比较上看,它们大概都可以实现30分钟到50分钟的检测,相对都是快的。这两个方法可以用试纸条的形式来读取结果,也很容易被大家所领会,不需要复杂仪器。
除了缩短时间,对于大规模的检测,提高检测通量是非常重要的,试剂盒可以拿来一盒就可以做好多检测,但是样品要一个一个测。还有核酸提取这样原来特别消耗体力而且需要经验、技巧、训练的工作,最好交给不知疲倦、不容易犯错的机器来操作。所以我们看到核酸提取自动化仪器大量出现在检测现场,这样的仪器遍布在各个定点医院,各级的疾控中心。

上图右边这两个仪器是在美国的大学实验室内,现在大学实验室大量加入到大规模检测的队列中来,能够消除一些检测滞后的焦虑。如果是一个集中处理的大型检测结构,就要用更加完整的自动化的仪器才好用。

上图是罗氏公司做的巨无霸仪器,Cobas8800,一台这样的机器,一天不停机大概可以完成3000个核酸检测,而且几乎全自动,把样品放进去之后就开始做。这有什么好处呢?除了快之外,还有一个重要的好处是可以保证在世界上不同地点,大家取得的结果都是基本可靠和稳定的。这样,在基础比较薄弱、积累不够雄厚的地方,一样可以实现高品质的大规模检测。在肯尼亚、在加拿大、在美国、在中国,得到检测结果不会由于操作问题而出现大的偏差。
随着疫情进展,越来越多的检测需求出现了。随着居家隔离变成常态,自我检测、自我采样能不能可行?在美国第一个获得药监局批准的居家自助采样试剂盒产品是LabCorp公司的产品Pixel,它用棉签在鼻腔中抹一下,然后寄回到检测中心做大规模检测,这样就不需要做很复杂的采样。
目前,还没有看到大规模的评价数据出现。但是毕竟拿棉签捅鼻子,是不太容易做到很好的稳定性的,所以一个多月前,华西医院的科研人员提出了用唾液进行新冠诊断的可能性。这是一个比较容易的自我采样的操作。
不到一个月前,美国耶鲁大学的科学家发表了一篇论文,比较了唾液和鼻咽拭子PCR核酸检测的效果。实验结果表明,和鼻咽拭子比,唾液采样的稳定性相当不错,甚至更好一些。另外更有意思的是绝大多数患者上看到的结果,唾液中检测的病毒更多一些,结果可能更加准确,减少假阴性的出现。这是一个很好的起点,所以前几天美国新泽西的Rutgers大学以及他们下属的检测机构获得了美国药监局的批准,开始使用唾液采集的样品来进行新冠病毒的检测。他们采用了一个流水线式的大规模处理的自动化机器,可以每天检测1万份样本。唾液采样检测是非常令人鼓舞的新方法,如果得到推广有望很好地解决我们过去采样中的面临的问题。
抗体检测
随着疫情的第一个高峰过去,复工复学的阶段到来,抗体检测成为新的流行语。
首先样本大不一样,都是用血或者血清进行的检测。抗体检测的方法多种多样,最常见的就是酶联免疫吸附和免疫化学发光法。这两个方法的原理非常像,也是实验室研究最常见的检测方式。以酶联免疫吸附检测原理为例,在检测基底上我们先铺一层人工制备的抗原,然后把血清样品加进去,孵育一段时间后,特异性结合到抗体上;然后我们把它洗脱,留下特异性结合的抗体;这时候加入酶标记的二抗,二抗能够识别免疫抗体,它上面还带催化作用的酶;然后再孵育一段时间,洗脱后留下特异性的二抗,加入一个底物会发生酶催化,从而导致显色反应的发生,使得溶液的颜色深浅发生变化。最终我们用产生显色反应的物质的浓度,推导出你想检测的抗体的浓度。这种方法,原理简单,特异性通过抗体识别来保证,不需要特别复杂的操作,可以自动化或者半自动化,实验通量不低。
另外一个方法是利用胶体金显色进行的试纸检测方法,检测是否怀孕的试纸用的也是类似的方法。这个方法的好处是非常简单、易用、便宜,而且不需要复杂的设备,速度非常快。

上图是试纸条的结构:样品垫、胶体金结合垫、醋酸纤维素膜和吸收垫。如果要检测的样品包括你想检测的抗体,比如新冠病毒的抗体IgM或者IgG,将样品送入试纸,这时候在胶体金结合垫上有金标抗原、金标单抗,即胶体金联合的抗原和单抗,一起向质控线方向流动,金标单抗会结合到金标单抗的抗体上,作为质控的结果。如果这个样品里面有这两个待测抗体,它就会加到这两个检测线上,同时由于它能够吸附金标抗原,所以会显色。如果显色了,就知道是否样品中存在待测抗体。如果IgG这条线很深,就知道有IgG;而IgM这条线显色非常浅,可以认为也许没有这个抗体,这个结果能够很简单地看懂。
为什么要做胶体金显色检测,是因为这个实验可以应用于大规模筛查。很多地方要调查感染率,如果感染率高,多数人有抗体,那这个病毒就不容易传播。如果感染率很低,大多数人没有抗体,病毒就很容易传播,这是为了更好地预防下一次的流行。
改进检测
那么做了检测就能得到想知道的结果吗?这需要非常认真地思考,因为没有一个方法是完美的。分子检测从来都不是完美的,这世界上没有完美的检测方法。要了解每一种检测方法的优势和缺点,以便更好地选择和判断。
首先,检测的时间点非常重要。

上图是前几天《美国医学会志》上刊登的一个示意图。不同的检测对象和疾病进展间的关系有很大不同。病毒在发病前几天才容易分离出来,那时候核酸载量是不多的。核酸检测能检测到吗?咽拭子或者肺泡的灌洗液要比粪便检测容易一些,但是粪便可能存在的时间长一些,后期更容易检测出来。抗体都是在发病后期才出来的,IgM抗体衰退比较快,IgG抗体衰退的慢,停留的时间会长一些。所以选择什么样的检测方法,跟时间节点有极其重要的关联性,每一个方法有极限。
我们在分析中经常用检出限来表示检测方法的灵敏度,检出限就是在给定的置信度条件下可以从被测样品中检测待测组分的最小浓度或者最小量。比如基因编辑方法检测技术跟传统的计算方法比,检出限比传统的RT-PCR方法高一个量级左右。实际上现在大量使用的RT-PCR的检测限非常低,也就是说检测的敏感性非常高,大概在一个反应能够检测几个核酸片断的存在。绝大多数其它检测方法,快的也好、慢的也好,不见得敏感性更好。
另外,要考虑一个检测方法的特异性是否真的很好。核酸检测中特异性取决于引物选择的位置、引物序列与目标核酸的匹配,还要考察是否真的能检测出来。来自香港科学家的这篇发表在《临床化学》的研究论文表明,两个核酸检测位点总,有一个位点明显比另一个更加容易检测出来,具体说就是N蛋白基因比ORF1b更容易检测出来,虽然一开始设计上看好像这两个位点的表现都差不多,但是真正使用的时候是有区别的。
虽然方法都不是完美的,但是它也有一定的可取之处,只要用的妥当,找到好的适用场景。真实感染者检测出来了,是真阳性;健康人被算成感染者,是假阳性;健康的人检测出来健康,是真阴性;感染者未被检测出来,是假阴性。所以真阳性、假阳性、真阴性、假阴性加在一起构成了整个检测样本的总数。
怎么评价?第一个评价指标:敏感性。所有的阳性样本中到底检测出几个阳性?分子是真阳性,分母是真阳性和假阴性的和。
另一个指标:特异性,也就是阴性的样本中有多少个真阴性。真阴性和假阳性一起当分母,而分子是真阴性。
很多场合我们都关心阳性结果是否真的是阳性?这就是所谓的阳性预测值(PPV)。
我们想象一下如果敏感性和特异性这俩指标没有那么高的情况吧。假设有一个大城市,感染率为1%,我们做一个1000人的抗体检测。所用的检测试剂敏感性90%、特异性80%,这个值符合现在不少试剂的真实指标。那会有什么样的结果呢?1000人里面,因为感染率是1%,所以真正有抗体的人应该有10个,没有抗体的人有990个。这10个人里面,由于检测试剂的敏感性是90%,所以有9个检测出来是真阳性,1个是假阴性。在没有抗体的人里面,因为检测的特异性是80%,所以其中990个人里面有792个被测成真阴性,但是198个人出现了假阳性。所以,检测结果出来后是这样的,测了1000人,结果207个呈现阳性,793个阴性。这说明一个人如果测到阳性结果,实际上只有4%的几率是真阳性,有96%的可能性并不是阳性。
怎么改变这个状态呢?根本的解决方法就是把试剂做的越来越好,比如说再增加一些特异性。假设特异性增加到90%,这个结果就变了,假阳性减少到99个人。但是这个结果,阳性预测率只从4%提高到8%,阳性结果中还是有90%以上的假阳性。假设特异性增加到99%,阳性预测率可以增长到47%左右。99%的特异性对抗体检测来说是很大的难题,因为这已经是非常高的指标了。这也是为什么检测能力不够理想的抗体检测在感染率低的情况下做大规模筛查是有很大问题和风险的,我们一定要把统计学的基本概念牢牢记在心里。
前几天美国加州的一帮科学家联合在一起组织了互助合作社,他们横向比较了不同的抗体检测方法,共进行了12种方法,10种是试纸条,2种是酶吸附。试纸条里面很多是中国厂商的产品,也有美国厂家的产品,结果看上去都差不多,并没有哪个特别一枝独秀。所以并不是说大家生产能力差别很大,而是这个方法的挑战本身是普遍性的。

可以发现这些方法都相当不错,他们的方法稳定性都相对不错,只不过现在为止没有哪个方法真的具备和核酸检测一样稳定和优秀的特异性,不能完全相信它的结果,所以抗体测试,尤其是胶体金测试中,总体上看,假阳性率是一个大问题。
最后花点时间讲讲是否有超越核酸检测的其它检测方法,比如测序。测序是过去几年才被大家提上日程的检测方法。过去几个月,我们正好有一个方法基本成型了,1月份的时候我、清华的王建斌和我们中心谢晓亮教授一起发表了一篇论文,是由狄琳和傅语思两个同学主要完成的。这个论文中报道了一个新的简便的RNA测序的处理方法,取名SHERRY。把样品放进去之后,用三步法就形成了测序,大大降低了以前这些对实验技巧要求非常高的实验操作的难度,可以使实验结果更加稳定、可靠和快捷获取。在新冠病毒肆虐的时候,医院都在超负荷运行,医院的科研人员也没有太多时间去想复杂的操作流程,所以越简单的操作流程越有利于为临床新冠测序服务。
过去几个月,我们虽然不能全面复工,但是我们有幸和北京地坛医院的合作者一起,在SHERRY基础上开发了新方法,叫MINERVA,这个方法的出发点就是真从实际出发考虑,如何为临床服务。这个方法不怎么挑样本,咽拭子、痰、粪便都可以,经过提取之后建立第一步的SHERRY文库,再经过富集等步骤就会有一个新的文库做病毒全基因组测序。
通过这个测序我们研究了80多个样本的核酸序列,从中可以看到之前很多没有办法用简单的核酸PCR检测手段获取的信息。我们看到了很有趣的现象,比如很多样本在特定位点中都可能有不同的突变。这是一个全新的病毒,对这个病毒了解得越深刻,越有利于我们防控疫情,也为未来可能的威胁做好准备。


