欧盟药监局(EMA)12日宣布,mRNA(信使核糖核酸)疫苗,如辉瑞或Moderna疫苗,似乎对印度变种新冠病毒有效。

▲ BFMTV新闻台相关报道截图
欧洲药品管理局疫苗战略负责人卡瓦列里(Marco Cavaleri)在新闻发布会上表示:“关于mRNA疫苗针对B.1.617新冠变体有效性,欧盟监管机构评估数据令人鼓舞。”B.1.617这种双重变异病毒,正在印度境内迅速蔓延。
在此次疫情中,BioNTech/辉瑞以及Moderna研制的mRNA新冠疫苗可谓是许多国家的抗疫英雄。但事实上,mRNA疫苗技术的初衷是为了研发抗癌药物,而此次mRNA疫苗的成功也加强了许多人对该技术前景的信心。
mRNA疫苗的原理
mRNA疫苗是一种新型疫苗:mRNA 是“授人以渔”的指令,教会细胞如何制造出一种蛋白质/蛋白质片段(“刺突Spike蛋白”),从而触发免疫反应。
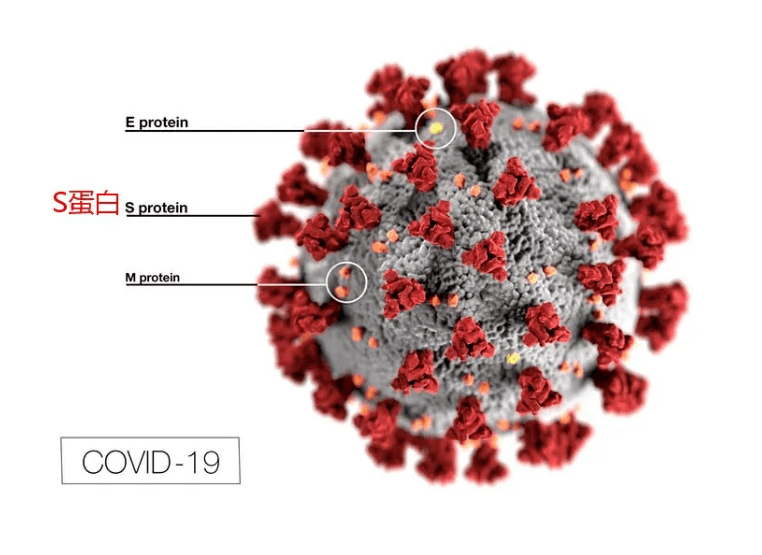
▲ S蛋白是新冠病毒入侵人体细胞的关键“钥匙”,mRNA疫苗是将编码S蛋白的基因直接注入人体,利用人体细胞在人体内合成S蛋白,刺激人体产生抗体。通俗的说,相当于把一份记录详细的病毒档案交给人体的免疫系统。
蛋白质片段形成后,细胞会分解指令并将其去除。接下来,细胞将蛋白质片段显示在其表面。我们的免疫系统认识到蛋白质不属于那里,并开始建立免疫反应和制造抗体。
这样,我们的身体就学会了如何防止未来的感染。
这种新技术并非不为人知
数十年来,人们对这种疫苗的兴趣日益浓厚,因为它们可以在实验室中使用现成的材料来开发。这意味着,过程可以标准化和规模化,使开发速度比传统方法更快。
法国CNRS研究人员皮塔德(Bruno Pitard)强调:“新冠疫情实际上为这种新型疫苗创造了机会,它的研发速度惊艳了所有人。”
但他也提醒人们谨慎,因为新冠确实是“教科书级别的案例”:鉴定抗原相对容易,而这部分也要归功于2002年针对非典病毒所做的研究。此外,产生的相关蛋白也能够诱发明显的免疫应答,因此,开发针对其他病毒的mRNA疫苗可能会比新冠疫苗更复杂!

▲ 人们在巴黎西郊一家新冠疫苗接种中心等待接种疫苗。(新华社图)
有望用于治疗癌症
除疫苗外,癌症研究还使用mRNA来触发针对特定癌细胞的免疫系统。
4月16日,瑞士苏黎世大学医院研究人员帕斯科洛(Steve Pascolo)在提到这一点时说道:“是的,这是二十年前开始的一场革命”、“还有一些障碍需要进一步改善,但是现在癌症信使RNA疫苗正在与其他疗法结合使用,并且显示出了优异的结果。”
▲ 瑞士苏黎世大学医院研究人员帕斯科洛表示:“我们很快将批准将抗癌mRNA疫苗与其他疗法结合使用。”(Franceinfo新闻台报道截图)
帕斯科洛介绍道,除了抗癌,“mRNA还有许多其他用途,比如治疗冠心病、皮肤病和一些遗传性疾病(...)所有这些潜在可能都正在开发中” 。
实际上,癌细胞会表达特定的蛋白质(TAA,与肿瘤相关的抗原),这些蛋白质由突变引起。同样身为 CureVac创始人之一的帕斯科洛总结道:“可以像生产令身体合成Spike蛋白的新冠疫苗一样,制造出能编码癌症相关蛋白的mRNA疫苗,从而使患者自身的免疫系统识别、杀死肿瘤细胞。”
因此,第一个研究思路是根据某些已知癌细胞蛋白(例如某些遗传性乳腺癌)来设计疫苗。但是更常见的是,相关蛋白质或抗原会根据不同患者体质而发生变化。因此,有必要对患者的癌组织进行活检,然后通过基因测序设计出“个性化”的疫苗。
早期诊断将仍是必不可少的,但随后mRNA相关治疗的进程是飞速的。
因为,只要制造出目标蛋白质的基因序列、而不再是蛋白质本身就足够了。例如,当中国于2020年1月11日公布了新冠病毒的基因序列后,Moderna只花了48小时就“完成了信使疫苗”。40多天后,就可以开始第一阶段试验。
但是,这种“定制”药物仍处于起步阶段,而目前生产mRNA药物的成本令人望而却步。
不仅如此, CureVac一项针对前列腺癌2期试验的失败,也凸显了“下注”的难度:“某些细胞总是会设法稍微改变其表面蛋白质,以便逃之夭夭”,帕斯科洛透露。
另一方面,狡猾的肿瘤细胞还会表达抑制剂,阻止我们的免疫细胞发挥作用。因此,mRNA药物面临的任务很艰巨,需要“全面开花”。
奥尔良大学分子和细胞生物学教授毕雄(Chantal Pichon)总结说:“mRNA必须在不同方面同时起作用:既作用于肿瘤细胞以阻断它们表达抑制剂,又要作用于人体免疫系统。”
新冠带来的商机?
好消息是,随着新冠疫苗的成功,研制mRNA药物的巨头们已经加大了研究投入。
▲ BioNtech公司于5月10日公布了今年第一季度业绩。因向全球供应新冠疫苗剂量迅速增长,该公司今年第一季度总收入估计超过20亿欧元,净利润达到11.28亿欧元。(法新社图)
1月份,分析公司Globaldata列举了44项正在进行的mRNA临床试验,其中一半致力于癌症研究,如BioNTech进行的黑色素瘤的2期试验;4月初,法国赛诺菲集团斥资1.6亿美元收购了英国初创公司Tidal Therapeutics,后者致力于肿瘤研究。
mRNA技术的无限潜力
对于mRNA技术,Moderna首席执行官、法国人班塞尔(Stéphane Bancel)还有其他实际应用设想,如为心肌梗塞患者提供改善血管重建的方案:在发作48小时内注射能编码VEGF蛋白的mRNA信使,该蛋白可促使干细胞形成新血管,以减缓心力衰竭现象。
班塞尔激动地写道:“全世界尚未意识到,我们可以创建那么多极其有效的产品!”

▲ Moderna首席执行官、法国人班塞尔(BFMTV新闻台截图)
事实上,可能性似乎是“无限的”。
如,CureVac公司与马萨诸塞州的一家医院合作进行眼部疾病疗法研究;TranslateBio希望对CFTR蛋白进行编码,以治疗肺囊性纤维化疾病。
帕斯科洛还提到了治疗视网膜变性或美容等领域的应用:“我们原则上可以编码制造弹性蛋白,这是一种在成年后不再产生的蛋白质”,他也热情地设想道:“对于每种疾病,理论上都有对应的信使RNA解决方案!”
美梦能否成真?
然而,法国CNRS研究人员皮塔德对这个设想持谨慎态度:“我们必须保持理性”,他回忆道,“在90年代,每个人都在谈论基因疗法,而30年后,我们仍然没能实现。”
无论如何,新冠疫苗的成功对相关研究者来说,是个天大的好消息。

▲ 瑞士苏黎世大学医院研究人员帕斯科洛透露,“几年前,当我做关于mRNA的演讲时,我总是要多准备几张幻灯片备用,因为没人提问,所以我只能多讲一会儿……(Franceinfo新闻台截图)
据奥尔良大学分子和细胞生物学教授毕雄介绍,此前mRNA“乏人问津”的原因在于,科学界“很久以前就认为,mRNA不能被应用,因为它不稳定、太容易降解了”,相比之下,单克隆抗体,病毒载体,基因疗法等则被认为更有价值。
然而法国又落后了……
总部位于图卢兹的Flash Therapeutics在2015年获得了一种名为“ LentiFlash”的mRNA载体专利:当Moderna或BioNTech使用脂质体时,这家法国初创公司已开发出将mRNA包装在人细胞膜和不含病毒基因的病毒衣壳中。
但讽刺的是,当Flash Therapeutics董事长布业(Pascale Bouillé)2018年与毕雄联合向法国国家投资银行BPI申请资助时,他们吃了闭门羹:“他们告诉我们,我们的研究还不够先进”,而如今mRNA研究确实已成为“香饽饽”。
相比德国,法国在这一潜力研究领域的技术还是有点落后:目前,只有美国和德国具备进行mRNA相关制剂的大规模工业生产能力。

▲ Moderna首席执行官、法国人班塞尔当时在法国工作时就认为mRNA大有可为,但这想法过于大胆,无法在法国施展拳脚。当时,剑桥mRNA研究团队力邀班塞尔加入。关于是否该辞职去美国,他妻子只说了一句话:“别像法国人那样思考问题。”于是,班塞尔辞职去了美国(LCI新闻台截图)
因此,法国科学家将在这一新的竞争领域加大投入。
毕雄透露, “免疫学和纳米医学这两个领域将会更密切合作”,并且“越来越多的同事希望从事mRNA研究、并与我们合作”。
3月底,法国纳米医学会的线上会议共召集了来自32国的500名参与者,其中包括许多法国人,而这在2年前是难以想象的。
这次,mRNA研究是真的要“起飞”了。


