在人类与新冠病毒的斗争依然胶着之时,中国科学家又传来好消息。
当地时间4月19日,由中国医学科学院秦川团队领衔,联合北京科兴生物技术有限公司等多家单位,在生物科学预印本论文平台bioRxiv发表了未经同行评审的研究论文。

图源:bioRxiv
研究团队通过试验规模生产,开发了纯化灭活的SARS-CoV-2病毒候选疫苗(PiCoVacc),该疫苗可在小鼠、大鼠及非人类灵长类动物中诱导SARS-CoV-2特异性中和抗体。
这些抗体有效中和了10个代表性病毒株,表明对全球流行的新型冠状病毒株的中和能力更广泛。
恒河猴实验:高剂量组7天后肺部病毒消失
为了评价纯化灭活毒疫苗PiCoVacc的免疫原性,研究者注射不同剂量制剂在小鼠体内,并在第0、7天再完成2次注射,未出现不良反应。
随后研究者在感染新冠病毒的恒河猴中做了攻毒实验。
首先,研究者在第0、7、14天通过中等剂量或高剂量给恒河猴接种3次疫苗。
结果显示,接受2种剂量注射的恒河猴,在第3周体内便出现中和抗体,第3周仍有增加,滴度与恢复期新冠肺炎病人血清水平接近。
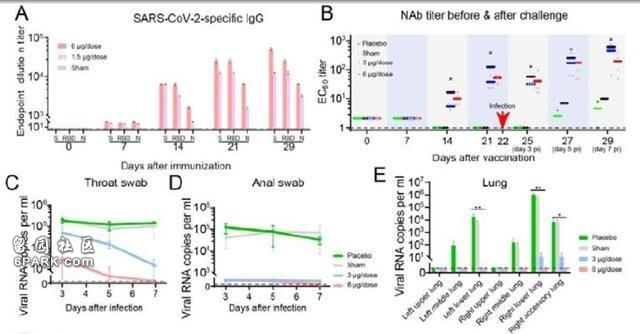
PiCoVacc在非人类灵长类动物中的免疫原性和保护功效
图A为接种后抗体反应;图B为恒河猴体内中和抗体滴度;图C、D、E分别代表恒河猴不同器官病毒载量,蓝色为中等剂量组,粉色为高剂量组。
接种病毒后第3-7天,对照组的恒河猴患上严重肺炎,而接种过疫苗的恒河猴,肺部组织病理变化明显减小。
在体内病毒载量的对比中,感染后第7天,高剂量组4只恒河猴的咽喉、肛门和肺部均检测不到病毒;中剂量组感染后第7天,各器官标本中能部分检测到病毒,但与对照组相比,病毒载量下降近95%。
此前开发SARS和MERS冠状病毒候选疫苗的经历,让大家对疫苗安全性(即可能引起ADE效应)产生担忧。
而在此实验进行到第29天时,评估了接种疫苗恒河猴各器官病理学后,研究团队认为疫苗没有引起显著的病理学特征,这也论证了其在恒河猴中的安全性。
作者团队曾研发全球第一支甲型H1N1流感疫苗
值得一提的是,该文章的作者之一——北京科兴生物制品有限公司,是中国首家在北美上市的中国疫苗企业科兴控股的控股子公司,此前,该公司曾研制出全球第一支SARS病毒灭活疫苗(完成I期临床研究)、全球第一支甲型H1N1流感疫苗和中国第一支大流行流感(H5N1)疫苗。
同时,该公司旗下另一子公司北京科兴中维生物研制的新型冠状病毒灭活疫苗(克尔来福),也在近日进入人体临床试验。
这一疫苗是用新型冠状病毒CZ株接种Vero细胞,经病毒培养、收获、灭活制成,目前首批志愿者已入组并完成第一针接种。
4月16日,志愿者接种科兴中维研制的新型冠状病毒灭活疫苗/图源:科兴生物官网
我国新冠疫苗研发:已有3个获批进入临床试验
当前各国都在加速新冠肺炎疫苗研发,而中国走得最前。
据科技司司长吴远彬介绍,目前我国获批进入临床的疫苗有三个,其中陈薇院士团队的腺病毒载体疫苗第1个获批,已于3月底完成Ⅰ期临床受试者的接种工作,并于4月12日开展Ⅱ期临床研究,世卫组织官网称,这是全球第一个启动Ⅱ期临床研究的新冠疫苗品种。

陈薇院士与84岁高龄的受试者合影/图源:现代快报
4月12日,国家药监局批准了武汉生物制品研究所、武汉病毒研究所联合申请的新冠病毒灭活疫苗,也进入了临床试验,志愿者已经接种疫苗。
13号,北京科兴中维生物技术有限公司研制的灭活疫苗开展临床试验。
获批进临床的速度这么快,疫苗安全吗?
从4月起,3个新冠病毒疫苗已经过应急审批进入临床,在振奋人心的同时,质疑的声音也随之出现:疫苗的安全性如何保障?
对此中国工程院院士王军志表示,疫苗的安全性与临床前的相关动物实验研究直接挂钩,其中包括急性毒性实验、重复毒性实验,以及动物攻毒试验,这些实验都要达到一定要求,才能获批上临床。

而对于疫苗什么时候能被接种,中国疾控中心主任高福表示,如果按正常的流程走,可能要到今年年底、明年年初才能出来。他还补充,根据疫情发展情况,在应急时可能会给一部分医务人员先使用疫苗,时间大概在年底。
据悉,全球已有70多个新冠疫苗研发项目正在进行,相信有效安全的疫苗一定能早日问世,让我们一起静待好消息的到来。
相关报道:中国披露全球首个新冠疫苗非人灵长类实验结果:有效、安全
临床上,目前人类对于新型冠状病毒(SARS-CoV-2)还没有特效药物,因此研发疫苗被寄予厚望。虽然新冠疫苗用于人体仍需等待,但中国科学家近日发表了首个新冠病毒非人灵长类疫苗实验结果,指出一种纯化灭活的候选疫苗能够为非人类灵长类动物提供完全保护,在有效性、安全性上均表现出积极结果。
当地时间4月19日,中国医学科学院医学实验动物研究所所长秦川等多个科学家团队,联合在生物科学预印本论文平台bioRxiv发表了研究文章“Rapid development of an inactivated vaccine for SARS-CoV-2”。
该文章作者来自北京科兴生物制品有限公司、中国疾病预防控制中心传染病预防控制所、北京协和医学院比较医学中心、中国科学院生物物理研究所感染与免疫院重点实验室等多个重点科研单位。
文章的通讯作者也包含多位传染病病毒、疫苗研究领域的顶级专家,包括早在2003年非典疫情期间就负责动物模型科研项目的秦川、浙江省疾控中心微生物检验所所长张严峻、北京科兴生物制品有限公司尹卫东、中科院感染与免疫重点实验室研究组长王祥喜、中国食品药品检定研究院呼吸道病毒疫苗室主任李长贵以及中国疾病预防控制中心传染病预防控制所党委书记卢金星。
研究团队通过试验规模的生产得到了一种纯化灭活的SARS-CoV-2病毒候选疫苗,名为PiCoVacc。他们发现,PiCoVacc能够在非人类灵长类动物中引发有效的体液免疫应答,对当前正在全球肆虐的SARS-CoV-2病毒株提供完全保护。
通过对恒河猴临床体征、血液学、生化指标等的系统分析,研究人员认为,该疫苗是安全的。
结合实验结果,研究人员表示,该疫苗可在小鼠、大鼠和非人类灵长类动物中诱导SARS-CoV-2特异性中和抗体,且在恒河猴体内未观察到感染增强或免疫病理恶化,将为用于人类的SARS-CoV-2疫苗的临床开发提供基础、指明方向。
值得注意的是,疫苗的研发虽被寄予厚望,但仍需时间进行科学的流程。就在4月20日,对于疫苗研发的时间表,中国疾控中心主任、中国科学院院士高福表示,如果按照正常的流程走,可能要到今年年底、明年年初才能出来。他还透露,根据疫情走势,在应急情况下,可能会于年底给一部分人群如医务人员先行使用新冠疫苗。
接种后6至7周抗体反应达到峰值,病毒RBD是主要免疫原
当前, SARS-CoV-2疫苗正在多途径紧急开发中,国内已有3个疫苗获批进入临床试验,其中一款腺病毒载体疫苗已经进入II期人体临床试验。
本实验中采用的纯化灭活病毒是疫苗开发的传统方法之一,这种类型的疫苗此前已被证明对于预防由流感病毒和脊髓灰质炎病毒等引起的疾病是安全有效的。
研究者从11名中国、意大利、瑞士、英国、西班牙等新冠肺炎确诊患者的支气管肺泡灌洗液中分离出了新冠病毒毒株,包含新冠病毒毒株的11个样本广泛分布在所有可用基因序列构成的系统发育树上。研究人员选择了其中一个毒株,开发出了纯化灭活的SARS-CoV-2病毒疫苗PiCoVacc。
遗传稳定性测试显示,PiCoVacc具有出色的遗传稳定性,不存在任何可能潜在改变NAb表位的S突变。
为了生产用于动物研究的试验规模的PiCoVacc,研究人员将其在50升Vero细胞培养物中繁殖,并使用β-丙内酯灭活。此后通过深度过滤等手段,研究团队得到了用于实验的高纯度的PiCoVacc制剂。

PiCoVacc的表征,图A为SARS-CoV-2最大似然系统树,图E为其低温电镜(cryo-EM)图像,它是直径为90-150 nm的完整椭圆形颗粒,上面缀有冠状尖峰,代表其预融合状态
为了评价PiCoVacc的免疫原性,研究者对小鼠进行了不同剂量的PiCoVacc注射,佐剂为明矾。研究人员在第0天和第7天进行了两次注射,未观察到炎症和不良反应。
在初次接种后的第1至6周,研究人员通过酶联免疫吸附测定(ELISA)评估了小鼠体内的S蛋白、受体结合域(RBD)和N特异性抗体反应。
结果显示,接种疫苗后,小鼠体内SARS-CoV-2的S蛋白和RBD特异性的IgG(免疫球蛋白G)迅速发展,在第6周达到峰值。
其中,RBD特异性的IgG占S蛋白抗体反应的一半,这表明RBD是主要的免疫原,这一结果也与恢复期的新冠肺炎患者的血清学特征相匹配。
此前的研究表明,N特异性IgG在新冠肺炎患者的血清中大量存在,并且是临床诊断标记之一。但出人意料的是,在这项实验的免疫小鼠中, N特异性IgG诱导的病毒S蛋白抗体反应量比靶向病毒S蛋白或RBD的抗体低约30倍。
此外值得注意的是,与恢复期COVID-19患者血清相比,PiCoVacc诱导出了更高滴度的S蛋白特异性抗体。事实上,针对新冠病毒N蛋白的抗体并不能提供针对感染的保护性免疫力,这些结果表明,PiCoVacc能够引发更有效的抗体反应。
接下来,研究者使用微中和测定(MN50)检测SARS-CoV-2特异性中和抗体在一段时间内的水平。结果显示,与S特异的IgG反应相似,高剂量免疫的中和抗体在第一周出现,在第二周加强免疫后显著增加,在第7周达到峰值,而对照组则未检测到SARS-CoV-2特异性抗体反应。
研究人员随后在大鼠身上进行了相同的免疫实验,并对不同毒株进行了中和测定,均得到了相似的结果。
恒河猴攻毒实验:高剂量组7天后肺部检测不到病毒
随后研究者在新冠病毒感染的恒河猴中进行了攻毒实验,以评估其免疫原性和保护功效。
首先,研究者在第0、7和14天通过中等剂量(每剂3μg)或高剂量(每剂6μg)给恒河猴接种三次疫苗。
结果显示,接受两种剂量注射的恒河猴体内新冠病毒S蛋白特异性的IgG和中和抗体均在第2周被诱导出来,并在第3周继续增加,滴度与恢复期的新冠肺炎患者的血清水平相似。

PiCoVacc在非人类灵长类动物中的免疫原性和保护功效,图A为接种后SARS-CoV-2-特异性IgG反应;图B为接种后和感染后恒河猴体内中和抗体滴度;图C、D、E分别代表恒河猴咽部、肛门和肺部的病毒载量,蓝色代表中等剂量组,粉色代表高剂量组
值得注意的是,疫苗剂量带来的中和抗体水平可能受个体差异影响。排除掉个例的影响后,中等剂量组恒河猴的中和抗体水平比高剂量组低约34%到40%。
随后,研究者在第22日进行攻毒(通过气管内途径将新冠病毒毒株直接接种到动物肺中)。
接种病毒后第3至7天,对照组的恒河猴表现出严重间质性肺炎,而与对照组相比,接种过疫苗的恒河猴病毒肺部组织病理变化显著减小。
此外,接种了疫苗的恒河猴体内病毒载量也显著下降。高剂量组的4只恒河猴感染后的第7天,它们咽喉、肛门和肺部就都检测不到病毒了;中剂量组感染后第7天咽部、肛门和肺部标本中能部分检测到病毒斑点,但与对照组相比病毒载量降低了约95% 。
论文还显示一个细节,接种了疫苗的恒河猴体内的中和抗体滴度在感染3天后下降了约30%,随后在感染后第5至7天水平迅速上升,以保持其有效的中和病毒效果。
排除个体差异影响后,与高剂量组相比,中等剂量组在感染后第7天有更高的中和抗体滴度,这可能是由于病毒复制水平较低,需要更长的时间才能完全清除病毒。
虽然研究人员观察到在感染前,中等剂量组体内存在较低的中和抗体滴度,可能提供部分保护,但任何接种过疫苗的恒河猴均未观察到病毒感染抗体依赖性感染的增强(ADE)。
PiCoVacc在恒河猴中具有安全性:感染未增强、无免疫病理恶化
此前开发SARS(严重急性呼吸综合征)和MERS(中东呼吸综合征)冠状病毒候选疫苗的经验引起了人们对肺部免疫病理学的担忧,这些疾病由辅助型T细胞2(T helper 2 cell,Th2)反应直接引起,或者由ADE引起。
尽管许多疫苗引起的T细胞反应对于急性病毒清除至关重要,但防止后续的冠状病毒感染主要是通过疫苗对体液免疫的介导。
临床上已经表明,由过度的T细胞反应引起的“细胞因子风暴”加剧了新冠肺炎的发病与患者多器官衰竭。因此,研究者们表示,SARS-CoV-2疫苗引起的T细胞应答必须被很好地控制,以避免免疫病理的发生。
基于这一前提,研究者们又通过观测临床指标和生化指数对于该疫苗的安全性进行验证,他们发现,所有接种疫苗的恒河猴均未发现发烧和体重减轻现象,且食欲和精神状态都保持正常。
在血液和生化分析方面,接种了疫苗的恒河猴的淋巴细胞亚群比例(CD3+、CD4+ 和CD8+)以及关键细胞因子(TNF-α、IFN-γ、IL-2、IL-4、IL-5和IL-6)表明与对照组相比均没有显著变化。
此外,第29天对接种疫苗的恒河猴的肺、心、脾、肝、肾和脑在内的各种器官组织的病理学评估表明,PiCoVacc没有引起显著的病理学特征,这些结果表明了PiCoVacc在恒河猴中具有安全性。
研究人员最后表示,尽管现在还不能确定相关研究中SARS-CoV-2感染的最佳动物模型,但感染SARS-CoV-2后产生类新冠肺炎症状的恒河猴似乎是研究该病的较为适用的动物模型。


