新冠疫苗生产研发大厂辉瑞制药的CEO竟然被检测出新冠阳性,这件事在昨日曝光后就登上了热搜榜。
如何形容此次事件背后的黑色幽默意味,我想不亚于生产老鼠药的工坊闹开了鼠疫。
疫苗、特效药,辉瑞从来都走在抗击新冠的前锋梯队,CEO的感染让看客开始揣测其下产品的作用。
屋漏偏逢连夜雨,早在十天前,哈佛医学院就在预印本上发表论文,公布了一项针对辉瑞目前卖的火热的特效药Paxlovid的研究,研究结果表明人们发现一些本应被Paxlovid治愈的新冠患者,出现了病情反复和核酸/抗原检测复阳。其中,最出名的案例是美国总统拜登和美国总统首席医疗顾问福奇博士。

Paxlovid
特效药不好用了?
复阳“魔咒”
2022年7月30日,白宫总统医生凯文·奥康纳发布书面信件,表示美国总统拜登新冠“复阳”。
此前,7月21日,白宫发布声明称,拜登新冠病毒检测阳性。在当时,拜登已完成疫苗全程接种,并接种了2针加强针。白宫表示,拜登将服用辉瑞抗病毒口服药Paxlovid用于治疗。 随后7月27日,白宫宣布拜登新冠病毒检测结果转阴。
随后,拜登连续4次新冠病毒检测阴性后,于第五天再次检测为阳性,但没有再次出现症状。白宫总统医生表示,目前没有理由对拜登进行新一轮治疗,但会重启严格的隔离程序。
拜登的经历并非个案。白宫总统医生凯文·奥康纳在最新的书面信件中同时提到,少数接受Paxlovid 治疗的新冠患者存在复阳的可能。
这一结果在哈佛医学院的新研究论文中的到了验证。
Paxlovid是一种蛋白酶抑制剂,由nirmatrelvir和ritonavir两种主要成分组成。其中nirmatrelvir是一种新冠病毒3CL蛋白酶抑制剂,能通过阻断新冠病毒3CL蛋白酶的活性,破坏新冠病毒的后续RNA复制过程。另一种成分ritonavir则让nirmatrelvir能在身体里保持更长时间的活性,更好地抗击病毒。
辉瑞的临床研究表明Paxlovid可降低已接种疫苗和低风险的新冠感染者重症率,有效抑制新冠病毒复制,但是,近期相继报道了mRNA新冠疫苗接种者在感染Omicron后采用Paxlovid治疗后发生反弹,且复阳症状、病毒载量和病毒持续时间等指标均比复阳前急性感染期严重,导致新冠特异性免疫受损。
最近的队列研究表明,普通mRNA疫苗接种人群新冠感染后复阳的概率为6%。然而,尚无研究探索mRNA疫苗接种人群接受Paxlovid治疗后的复阳概率及Paxlovid反弹现象的原因。
而此项研究以2022年3月至5月期间在美国马萨诸塞州36名接种mRNA疫苗后感染奥密克戎的患者为研究对象,其中11人接受了Paxlovid治疗。研究人员连续14天对研究对象进行鼻拭子采样,分析病毒载量和基因组测序数据。并通过调查问卷了解36名研究对象的既往病史、COVID-19疫苗接种情况和症状等个人信息,最终得出结论:与未接受Paxlovid治疗的新冠患者相比,Paxlovid治疗与更高的病毒反弹发生率相关。
这项研究的几组数据值得关注:1、新冠复阳率:未服用Paxlovid组为4%,服用Paxlovid组为27%;2、反弹中位时间和病毒峰值:未服用Paxlovid组为5天Ct(Ct值越小表明病毒载量越高)=30.3,服用Paxlovid组为5天Ct=19。
药物抵抗,只是时间问题?
值得注意的是, 除了 Paxlovid,另一款新冠抗病毒口服药Molnupiravir 也在使用后报告了复阳情况。
据凯斯西储大学医学院的研究显示,Paxlovid和Molnupiravir 治疗后都有一定概率出现复阳,治疗 7 天后两种药物的有症状的复阳率分别为2.31%和3.75%,住院治疗的复阳比分别为0.44%和0.84%。
难道,复阳只是时间问题吗?
目前,已经有多篇论文着手研究新冠病毒突变与药物抵抗之间的关系,6月,《科学》上发表了一篇关于冠状病毒主要蛋白酶(MPro)结构的新论文,着眼于这种抗性变体可能在哪里发展。
作者鉴定了45-51位氨基酸,以及其他几个也会影响活性结合位点的残基(M165、L167、P168、R188 和 Q189)。(对于分子生物学领域以外的人,该符号使用单字母氨基酸缩写以及蛋白质序列中的编号位置。例如,“L50F”告诉您蛋白质第 50 位的亮氨酸氨基酸 (L) 已被苯丙氨酸 (F) 氨基酸取代)。
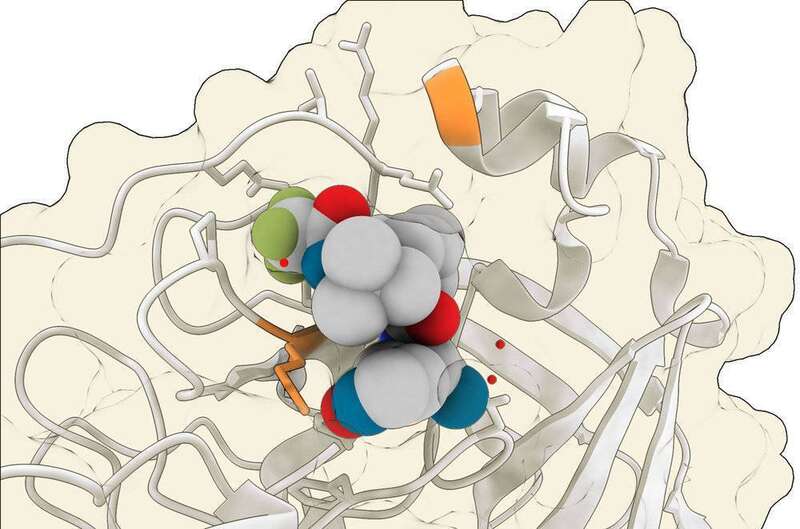
图:V. ALTOUNIAN/科学,数据:RCSB 蛋白质数据库,ID 7U28
在实验室研究中,一种冠状病毒蛋白酶上的几个位点(橙色)会发生突变,从而使病毒对 Paxlovid 中的活性成分(此处显示为蛋白酶中的灰色和彩色球体)更具抵抗力。
无论如何,这些样本量并不完全。结果显示,与小分子直接相互作用的蛋白质区域是 40-44、45-51、140-146、163-169和 86-192这些影响活性位点结构的蛋白质。
现在,任何这样的突变都可以在酶完成其工作的一般适应性与其逃避小分子抑制剂结合的能力之间进行权衡。肯定有很多突变会阻止Paxlovid 的蛋白酶抑制剂成分(尼马瑞韦)完全结合,但也会阻止许多酶的底物结合,所以这些在进化上是死胡同。
辉瑞自己的团队也做过类似的实验,但使用的是冠状病毒家族的另一个成员小鼠肝炎病毒 (MHV)。该预印本认为MHV不是一个很好的选择,因为nirmatrelvir从一开始就不是一个非常有效的抑制剂——作者认为,在像这样容易出错的复制系统中使用真正的SARS-2-CoV蛋白酶是调查突变的更好方法。
此外,在丹麦团队研究的试验中作者还研究了Vero细胞中的SARS-CoV-2。他们发现了L50F和E166V突变等,与野生型相比,这两种突变对nirmatrelvir 的耐药性高达 80 倍,同时具有较高的生殖适应性。E166V 突变本身的适应性较差,但通过在其上添加 L50F 突变来弥补这一点。这些作者指出,瑞德西韦的疗效不受这些突变的影响,并建议如果我们在普通人群中遇到不良耐药情况,可以同时使用使用两种药物。
将这些不同的论文放在一起,我们或许谈谈这些不同的突变体以及它们如何影响 nirmatrelvir 结合。研究人员认为,“Paxlovid 复阳”最大可能是由于药物暴露不足或持续时间不足导致。
所有的指向表明,冠状病毒的突变也是为了近一步影响药物的作用,但现在目前所有研究中都是针对部分片段展开,我们目前不能知晓病毒的哪些结构会促进这种逃逸。